Ikatan kimia
Jenis-jenis ikatan kimia
A. Ikatan Antar Atom
1) Ikatan Ion
 |
| Gambaran Ikatan Kimia Khusus Ikatan Ion |
- Pada suhu kamar berwujud padat;
- Struktur kristalnya keras tapi rapuh;
- Mempunyai titik didih dan titik leleh tinggi;
- Larut dalam pelarut air tetapi tidak larut dalam pelarut organik;
- Tidak menghantarkan listrik pada fase padat, tetapi pada fase cair (lelehan) dan larutannya menghantarkan listrik.
2) Ikatan Kovalen
NH3 + H+ → NH4+
- Pada suhu kamar berwujud gas, cair (Br2), dan ada yang padat (I2);
- Padatannya lunak dan tidak rapuh;
- Mempunyai titik didih dan titik leleh rendah;
- Larut dalam pelarut organik tapi tidak larut dalam air;
- Umumnya tidak menghantarkan listrik.
3) Ikatan Logam
Ikatan logam adalah ikatan kimia yang terbentuk akibat penggunaan bersama elektron-elektron valensi antaratomatom logam. Contoh: logam besi, seng, dan perak. Ikatan logam bukanlah ikatan ion atau ikatan kovalen. Salah satu teori yang dikemukakan untuk menjelaskan ikatan logam adalah teori lautan elektron.
Contoh terjadinya ikatan logam. Tempat kedudukan elektron valensi dari suatu atom besi (Fe) dapat saling tumpang tindih dengan tempat kedudukan elektron valensi dari atom-atom Fe yang lain. Tumpang tindih antarelektron valensi ini memungkinkan elektron valensi dari setiap atom Fe bergerak bebas dalam ruang di antara ion-ion Fe+ membentuk lautan elektron. Karena muatannya berlawanan (Fe2+ dan 2 e–), maka terjadi gaya tarik-menarik antara ion-ion Fe+ dan elektron-elektron bebas ini. Akibatnya terbentuk ikatan yang disebut ikatan logam.
Contoh terjadinya ikatan logam. Tempat kedudukan elektron valensi dari suatu atom besi (Fe) dapat saling tumpang tindih dengan tempat kedudukan elektron valensi dari atom-atom Fe yang lain. Tumpang tindih antarelektron valensi ini memungkinkan elektron valensi dari setiap atom Fe bergerak bebas dalam ruang di antara ion-ion Fe+ membentuk lautan elektron. Karena muatannya berlawanan (Fe2+ dan 2 e–), maka terjadi gaya tarik-menarik antara ion-ion Fe+ dan elektron-elektron bebas ini. Akibatnya terbentuk ikatan yang disebut ikatan logam.
B. Ikatan Antar Molekul
1. Gaya London (Dispersi)

Gambar 1. Gaya London

Gambar 2. Terjadinya dipol terimbas
2. Gaya Van der Waals
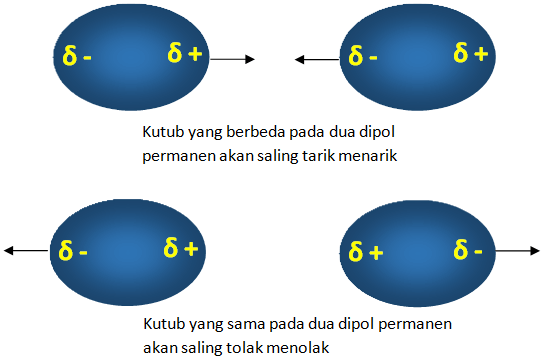
Gambar 3. Gaya Van der Waals pada dipol-dipol sehingga dinamakan gaya dipol-dipol

Gambar 4. Gaya ion dipol
3. Ikatan Hidrogen
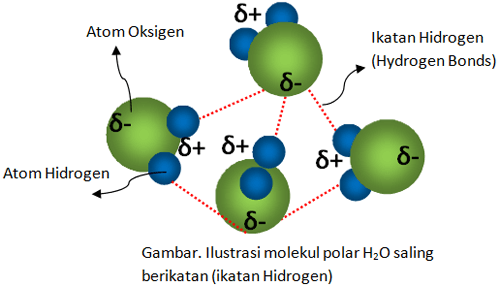
Gambar 5. Ikatan Hidrogen


2. Gaya Van der Waals


3. Ikatan Hidrogen











Keren
BalasHapusMantap
BalasHapusKeren
BalasHapus